Wenige Wochen vor der Präsentation seiner neuen Xbox Series X ist Microsoft ein wichtiger Schachzug gelungen. Die Kalifornier übernehmen den Videospiel-Konzerns Zenimax und zahlen dafür rund 7,5 Milliarden Dollar - in bar. Zenimax ist mit seinen Studios für Spielehits wie "Doom", "Fallout" oder "The Elder Scrolls" verantwortlich und hat laut eigenen Angaben rund 2.300 Mitarbeiter. mehr ...
Wenige Wochen vor der Präsentation seiner neuen Xbox Series X ist Microsoft ein wichtiger Schachzug gelungen. Die Kalifornier übernehmen den Videospiel-Konzerns Zenimax und zahlen dafür rund 7,5 Milliarden Dollar - in bar. Zenimax ist mit seinen Studios für Spielehits wie "Doom", "Fallout" oder "The Elder Scrolls" verantwortlich und hat laut eigenen Angaben rund 2.300 Mitarbeiter. mehr ...
Itzehoer Aktien Club

Corona-Impfstoff in Sicht
 24.09.2020
24.09.2020
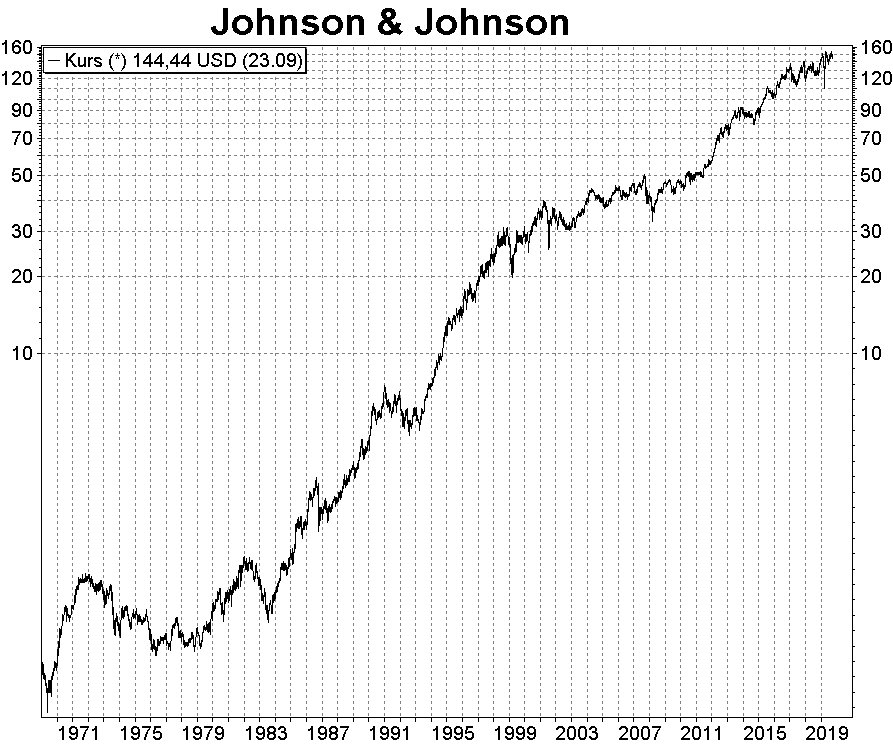
 Im Rennen um einen Corona-Impfstoff hat nun auch der US-Hersteller Johnson & Johnson die letzte und entscheidende Phase der klinischen Tests gestartet. In einer sogenannten Phase III-Studie mit bis zu 60.000 Freiwilligen auf drei Kontinenten sollen Sicherheit und Wirksamkeit des Impfstoffkandidaten überprüft werden. Inzwischen haben mehrere Hersteller die vor der Zulassung nötigen Massentests mit Zehntausenden Probanden gestartet. Darunter sind der britische Hersteller Astrazeneca, das deutsche Unternehmen BioNTech sowie das US-Unternehmen Moderna. Diese hoffen auf einen erfolgreichen Abschluss der Studien und eine Zulassung noch in diesem Jahr. Die meisten Hersteller gehen davon aus, dass für einen Schutz gegen das Coronavirus zweimal geimpft werden muss. Die Besonderheit von Johnson & Johnsons Mittel ist es, dass nur eine Dosis ausreichend Schutz bieten soll. Die Ergebnisse der bisherigen klinischen Tests seien positiv verlaufen, hieß es. Johnson & Johnson hofft, dass Anfang 2021 die ersten Dosen des Impfstoffs "für den Notfallgebrauch" zur Verfügung stehen.
Im Rennen um einen Corona-Impfstoff hat nun auch der US-Hersteller Johnson & Johnson die letzte und entscheidende Phase der klinischen Tests gestartet. In einer sogenannten Phase III-Studie mit bis zu 60.000 Freiwilligen auf drei Kontinenten sollen Sicherheit und Wirksamkeit des Impfstoffkandidaten überprüft werden. Inzwischen haben mehrere Hersteller die vor der Zulassung nötigen Massentests mit Zehntausenden Probanden gestartet. Darunter sind der britische Hersteller Astrazeneca, das deutsche Unternehmen BioNTech sowie das US-Unternehmen Moderna. Diese hoffen auf einen erfolgreichen Abschluss der Studien und eine Zulassung noch in diesem Jahr. Die meisten Hersteller gehen davon aus, dass für einen Schutz gegen das Coronavirus zweimal geimpft werden muss. Die Besonderheit von Johnson & Johnsons Mittel ist es, dass nur eine Dosis ausreichend Schutz bieten soll. Die Ergebnisse der bisherigen klinischen Tests seien positiv verlaufen, hieß es. Johnson & Johnson hofft, dass Anfang 2021 die ersten Dosen des Impfstoffs "für den Notfallgebrauch" zur Verfügung stehen.
Fazit: Das Impfstoffprogramm von Johnson & Johnson nutzt bewährte Technologien, die schon bei der Entwicklung des kürzlich in Europa zugelassenen Ebola-Impfstoffs des Unternehmens zum Einsatz kamen. Der COVID-19-Impfstoffkandidat basiert auf der AdVac-Technologie des Unternehmens. Diese wurde bereits für die Entwicklung der Zika-, RSV- und HIV-Impfstoffkandidaten verwendet, so dass bereits viele Sicherheitsdaten aus zurückliegenden Studien vorliegen. Damit besteht eine begründete Hoffnung, dass der Impfstoff wirksam und zugleich auch sicher ist.
Die folgende Firmen-News könnten Sie auch interessieren:
Microsoft kauft Spieleentwickler 22.09.2020
Daimler mit Großlieferung an Amazon 28.08.2020
 Der weltgrößte Onlinehändler bestellt in großem Stil Elektrolieferwagen von Daimler. Die Lieferung von mehr als 1.200 Transportern vom Typ eSprinter und rund 600 eVito-Stadtlieferwagen sei die bislang größte Order für Mercedes-Benz Van, teilten die Stuttgarter mit. Die Fahrzeuge sollten bereits ab diesem Jahr in mehreren europäischen Ländern eingesetzt werden. mehr ...
Der weltgrößte Onlinehändler bestellt in großem Stil Elektrolieferwagen von Daimler. Die Lieferung von mehr als 1.200 Transportern vom Typ eSprinter und rund 600 eVito-Stadtlieferwagen sei die bislang größte Order für Mercedes-Benz Van, teilten die Stuttgarter mit. Die Fahrzeuge sollten bereits ab diesem Jahr in mehreren europäischen Ländern eingesetzt werden. mehr ...
Alibaba als Corona-Profiteur 20.08.2020
 Online-Shopping und der Trend zum Homeoffice in der Corona-Krise spielen dem Amazon-Konkurrenten Alibaba in die Hände. Die chinesische Handelsplattform glänzt mit einem Umsatzsprung. Von April bis Juni stieg der Umsatz um rund 34 Prozent auf umgerechnet rund 18,8 Milliarden Euro. Dies lag über den Erwartungen von Analysten. Besonders stark legten die Einnahmen im Cloud-Geschäft... mehr ...
Online-Shopping und der Trend zum Homeoffice in der Corona-Krise spielen dem Amazon-Konkurrenten Alibaba in die Hände. Die chinesische Handelsplattform glänzt mit einem Umsatzsprung. Von April bis Juni stieg der Umsatz um rund 34 Prozent auf umgerechnet rund 18,8 Milliarden Euro. Dies lag über den Erwartungen von Analysten. Besonders stark legten die Einnahmen im Cloud-Geschäft... mehr ...
Nestlé macht uns gesund 18.08.2020
 Tiefkühlpizza, Getränke, Tierfutter, Babynahrung, Kaffee – der Nestlé-Konzern produziert in erster Linie Produkte für den täglichen Bedarf. Seit einiger Zeit sind die Schweizer aber auch bestrebt, Nahrungsmittel zu offerieren, die nicht nur gut schmecken, sondern zusätzlich auch einen medizinischen Nutzen haben. Gemäß dieser Strategie verleibt sich Nestlé nun mit IM HealthScience... mehr ...
Tiefkühlpizza, Getränke, Tierfutter, Babynahrung, Kaffee – der Nestlé-Konzern produziert in erster Linie Produkte für den täglichen Bedarf. Seit einiger Zeit sind die Schweizer aber auch bestrebt, Nahrungsmittel zu offerieren, die nicht nur gut schmecken, sondern zusätzlich auch einen medizinischen Nutzen haben. Gemäß dieser Strategie verleibt sich Nestlé nun mit IM HealthScience... mehr ...
Walt Disney verschiebt Filmstarts 27.07.2020
 Wann waren Sie das letzte Mal im Kino? Bestimmt können sich viele von Ihnen gar nicht mehr dran erinnern - so lang ist das schon her. Corona lässt grüßen. Dieser Umstand trifft natürlich vor allem die Kinobetreiber, aber auch die Filmproduzenten wie z.B. Walt Disney. Da weltweit nur wenige Menschen aufgrund der Corona-Beschränkungen ins Kino gehen können und wollen, hat der weltgrößte Medienkonzern gemeldet, dass er drei... mehr ...
Wann waren Sie das letzte Mal im Kino? Bestimmt können sich viele von Ihnen gar nicht mehr dran erinnern - so lang ist das schon her. Corona lässt grüßen. Dieser Umstand trifft natürlich vor allem die Kinobetreiber, aber auch die Filmproduzenten wie z.B. Walt Disney. Da weltweit nur wenige Menschen aufgrund der Corona-Beschränkungen ins Kino gehen können und wollen, hat der weltgrößte Medienkonzern gemeldet, dass er drei... mehr ...